En la última década, investigadores de todo el mundo han centrado sus esfuerzos en el desarrollo de tecnologías de baterías "más allá del litio" para aumentar, o en determinadas situaciones sustituir, las baterías de iones de litio. La demanda de energía es cada vez mayor y son necesarias nuevas soluciones que permitan el uso de energías renovables, posibilitando así una transición limpia hacia la descarbonización. En este escenario, las baterías de metal-oxígeno-aire (M-O2/aire) tienen la capacidad de desempeñar un papel importante en el desarrollo de aplicaciones tanto estacionarias como de movilidad, debido a su alta densidad energética teórica en comparación con los sistemas actuales.
La ventaja inherente a las baterías de metal-aire es que el material activo del cátodo se absorbe del medio ambiente circundante (O2), lo que confiere a las baterías de metal-aire una de las mayores densidades energéticas teóricas de todos los sistemas de baterías.
Entre las distintas químicas, la batería de Na-aire/O2 (NAB) es un candidato prometedor con una densidad energética hasta 6 veces superior a la de las baterías de iones de litio (LIB) (~1600 Wh kg-1 vs 250 Wh kg-1). Además, el sodio es el sexto elemento más abundante en la corteza terrestre, lo que supone una importante ventaja económica y de recursos, sobre todo si se combina con la posibilidad de utilizar un colector de corriente de aluminio, que reduce los costes generales de producción y el peso de la batería.
Peled et al. descubrió la primera NAB en 2011 y desde entonces los esfuerzos de investigación se han centrado en la comprensión de los mecanismos de reacción que se basan en la reacción de reducción de oxígeno (ORR) durante la descarga y la reacción de evolución de oxígeno (OER) durante la carga, además de investigar nuevos electrodos y electrolitos.
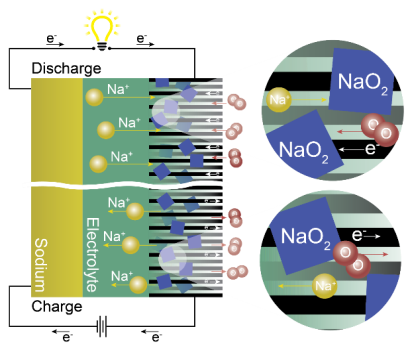
A diferencia de las baterías de iones de litio, que se basan en la química de intercalación (un catión se intercala en los electrodos), las NAB almacenan su energía mediante la llamada reacción de conversión. Esto significa que se forma un nuevo sólido, es decir, un óxido. Normalmente, la configuración de la batería consiste en un ánodo que contiene sodio, un electrolito orgánico conductor de sodio y un cátodo de aire (véase la figura). El mecanismo de reacción implica que el gas oxígeno se disuelve en el electrolito y forma O22-, que luego se combina con el Na+ para formar superóxido de sodio (NaO2) (Na+ + O2 + 1e- ↔ NaO2). También se han descrito otros productos de descarga, como el peróxido de sodio (Na2O2) y peróxido hidratado (Na2O2·H2O).