Abundancia y coste
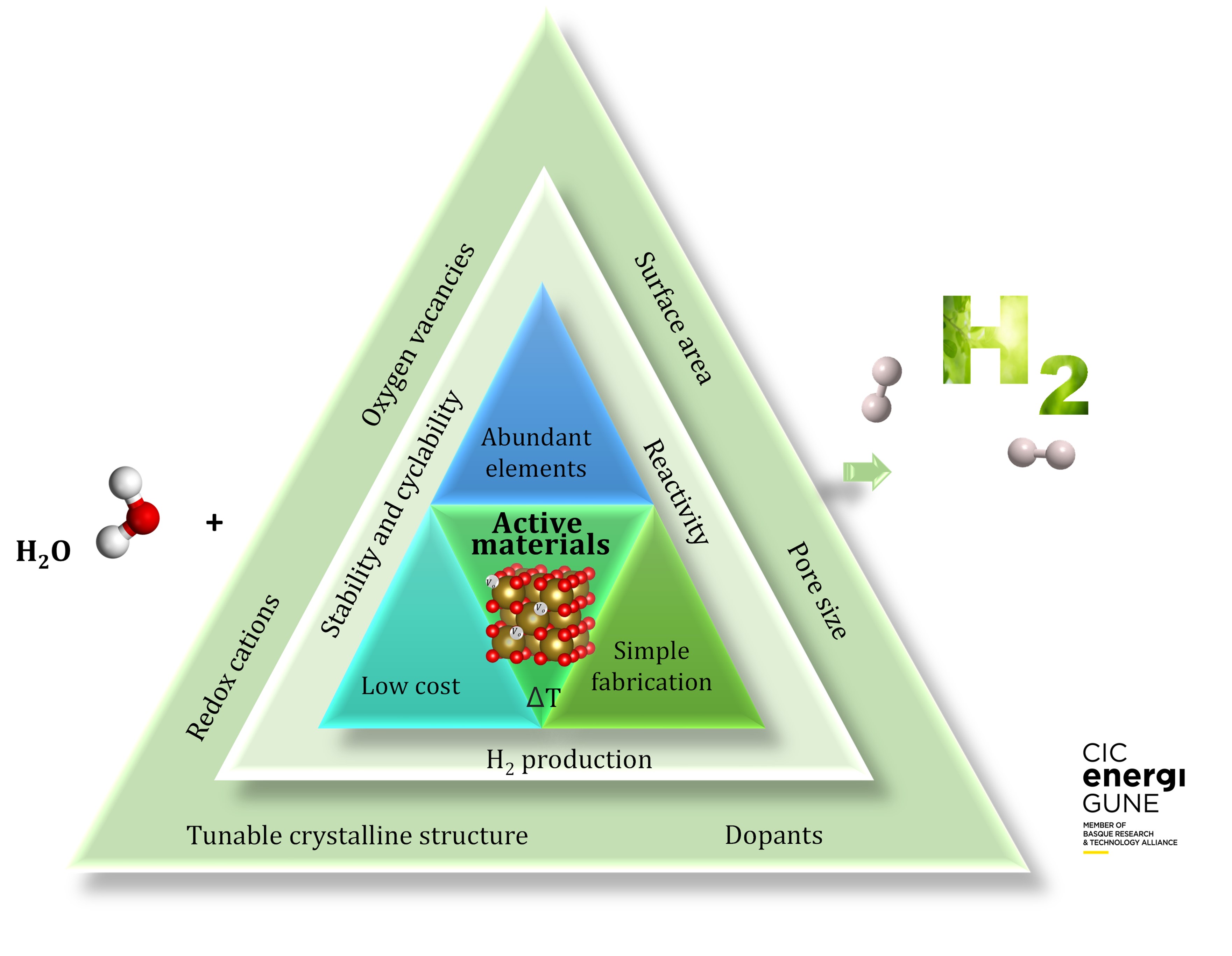
Para lograr un proceso escalable sostenible y rentable, se requieren materiales robustos basados en la tierra que muestren un alto rendimiento y ciclabilidad para la producción de H2.
Capacidad de intercambio de oxígeno
La cantidad de oxígeno liberado en la etapa de reducción depende de la capacidad de intercambio de oxígeno del material e influye en la cantidad máxima de combustible producido en la etapa de oxidación. La capacidad de intercambio de oxígeno viene definida por la no estequiometría (d).
El objetivo es disponer de materiales con una elevada capacidad de intercambio de oxígeno y una gran estabilidad durante un gran número de ciclos6.
Volátil - no volátil
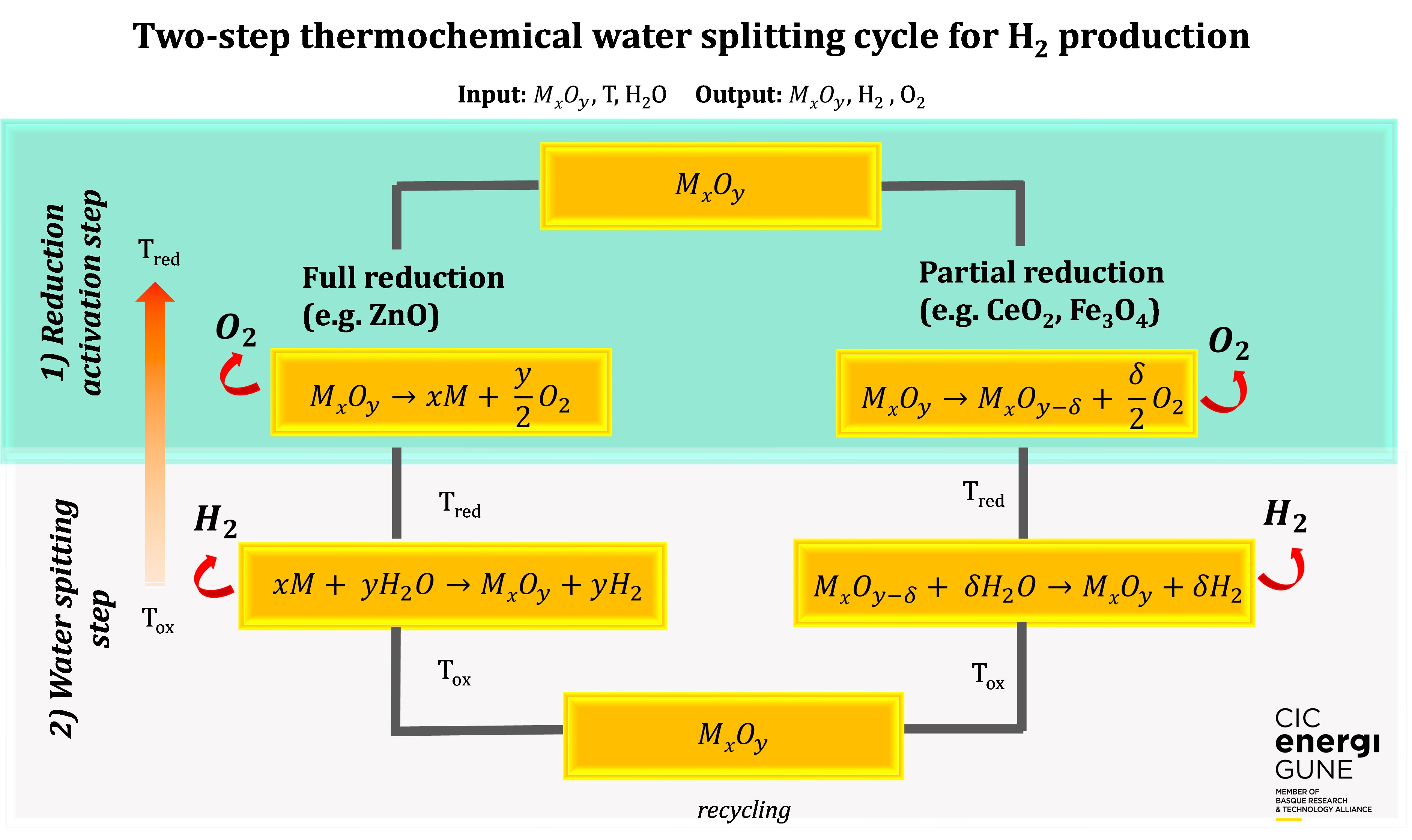
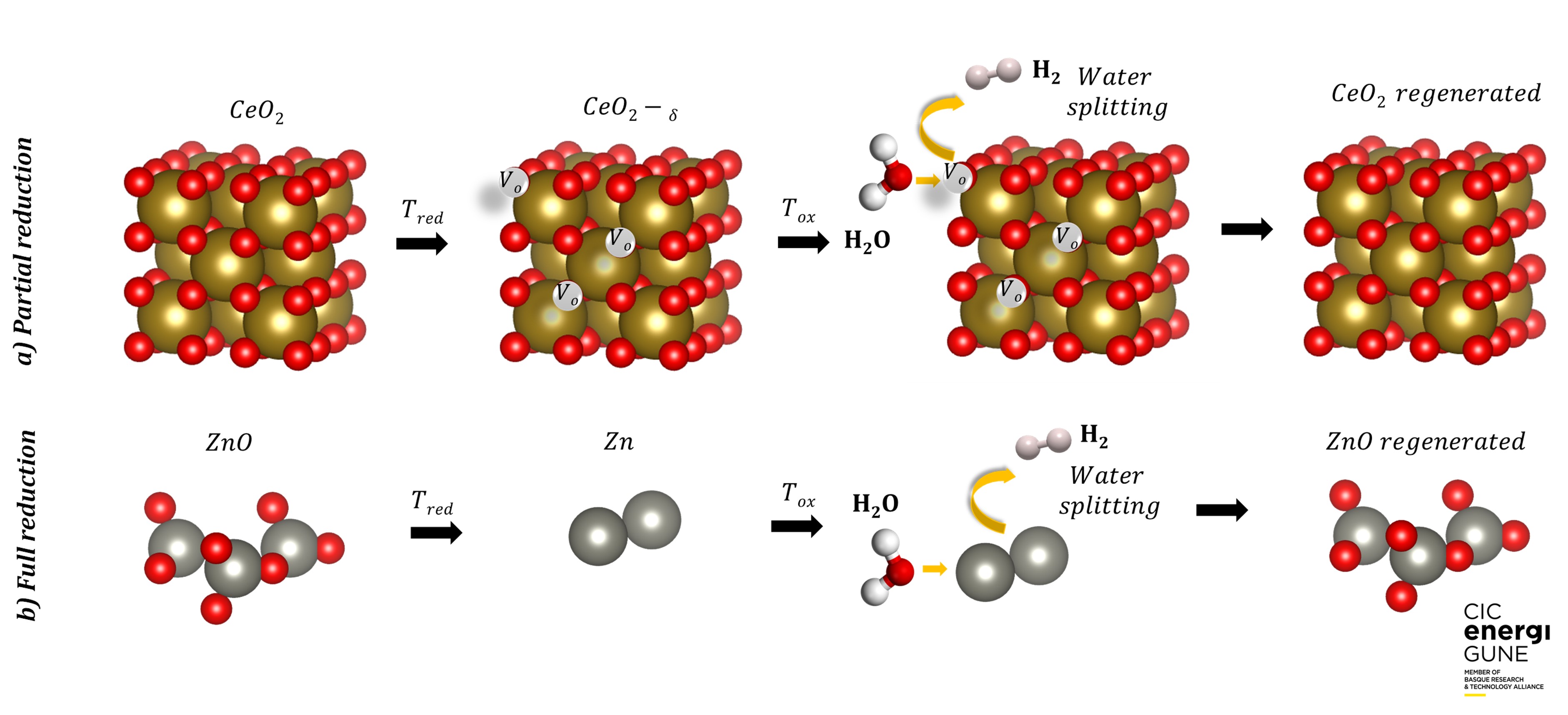
Los ciclos basados en óxidos metálicos pueden clasificarse en volátiles (por ejemplo, ZnO/Zn) o no volátiles (por ejemplo, Fe3O4/FeO), dependiendo de si el óxido experimenta una transición sólido-gas o permanece en fase sólida durante las reacciones. El oxígeno liberado y el combustible producido en los sistemas volátiles es mayor en comparación con los no volátiles. Sin embargo, tras la etapa de reducción, el material debe enfriarse para evitar la recombinación7.
Estequiométrico - no estequiométrico
Mientras tanto, los sistemas no volátiles pueden clasificarse en óxidos estequiométricos (por ejemplo, Fe3O4) y no estequiométricos (CeO2), y las propiedades termodinámicas y cinéticas de estos óxidos se ven afectadas por el dopaje o la sustitución por aniones y cationes. De forma general, los óxidos estequiométricos presentan una mayor liberación de oxígeno, pero su desventaja es una cinética lenta y una baja estabilidad estructural y química, lo que dificulta el rendimiento del material y limita la cantidad de combustible producido.7.
Estructura cristalina
Los materiales que ofrecen una estructura cristalina estable con composición sintonizable son muy atractivos, ya que ofrecen la posibilidad de dopaje y formación de vacantes de oxígeno sin transformación de fase tras las reacciones redox. Las familias más estudiadas son las perovskitas, las espinelas y los pirocloros, entre otras8.
Actividad redox
La capacidad redox está muy influida por la estructura electrónica del material, y los cationes de la estructura cristalina desempeñan un papel determinante durante las reacciones redox. Por ejemplo, los materiales con cerio, hierro, manganeso, lantano y otros metales de transición han mostrado una elevada reducibilidad. Sin embargo, un material ideal debe presentar unas propiedades termodinámicas y cinéticas adecuadas tanto para la reducción como para la oxidación, lo cual sigue siendo un reto, ya que no todos los materiales muestran una cinética de oxidación rápida.5.
Doping
Se ha estudiado en profundidad el efecto del dopaje en las propiedades de los óxidos metálicos para la separación termoquímica del agua. Por ejemplo, se ha demostrado que la sustitución del cerio por dopantes divalentes, trivalentes y tetravalentes de menor radio es beneficiosa para promover una mayor cantidad de oxígeno liberado. Mientras tanto, un dopante con mayor valencia y menor radio iónico favorece el grado de reducción de la ceria dopada, modificando los enlaces M-O de la estructura cristalina, que son más fácilmente rompibles en estas condiciones9.
Superficie y tamaño de los poros
Los materiales con estructura microporosa benefician la reacción de oxidación, debido a la elevada área superficial, mientras que los materiales con estructura macroporosa, con poros del orden de milímetros, favorecen el calentamiento homogéneo5. Además, se ha demostrado que el uso de nanopartículas mejora la producción de H2 debido a la mayor superficie expuesta, mejorando la cinética de reacción, la transferencia de calor y masa y la velocidad de reacción global. La Tabla 1 resume las ventajas de los materiales porosos para la división termoquímica del agua.
Tabla 1. Ventajas de los materiales porosos para la separación termoquímica del agua
| Característica |
No poroso |
Materiales porosos |
| Sinterización |
+++ |
++ |
| Cinética |
+ |
+++ |
| Homogeneidad calorífica |
+ |
+++ |
| Transferencia de masa |
++ |
+++ |
| Reactividad sólido-gas |
+ |
+++ |
| Caídas de presión |
+++ |
+ |
| Difusión de reactivos y productos |
+ |
+++ |
Perspectivas
En la actualidad, las principales limitaciones de los materiales activos para la separación termoquímica del agua están asociadas a la alta temperatura de reducción y a la baja producción de H2 y ciclabilidad de los materiales, debido a procesos no deseados como la sinterización, la baja reactividad y la formación de fases secundarias. Por esta razón, en CIC energiGUNE, estamos trabajando en el diseño y desarrollo de nuevos y competitivos materiales que puedan ofrecer una producción estable de H2 y una gran vida útil como perspectivas para su uso en la producción de H2 a gran escala.