Hidrogenoak gero eta zeregin garrantzitsuagoa du etorkizuneko munduko energia-ekoizpena eta -banaketa deskarbonizatzeko planetan. Bere funtzio garrantzitsuenetako bat bektore energetiko gisa da, hau da, energia garraiatzaile gisa energia iturri primario batetik behar den lekuraino. Hidrogenoaren abantaila nagusietako bat da erregai gisa erabiltzen denean, adibidez erregai-piletan, oso garbia dela. Ura da hondakin bakarra, eta ez ditu hidrokarburoen errekuntzan sortzen diren kutsatzaile kaltegarriak isurtzen; beraz, ezin hobea da hiri-inguruneetan erabiltzeko, garraio astunerako (autobusak, esaterako), eta beroa eta elektrizitatea konbinatuta produzitzeko instalazioetarako, etxeko eta merkataritzako eraikinetan.
Hidrogenoaren beste funtzio garrantzitsu bat lehengai kimiko gisa erabiltzea da; izan ere, hidrogenoaren egungo erabilera gehienak findegietan, ongarrietarako amoniakoaren ekoizpenean eta altzairuaren ekoizpenean ematen dira. Energiaren Nazioarteko Agentziaren (AIE) arabera, 74 milioi tona hidrogeno ekoitzi ziren mundu osoan 2018an. Gaur egun, hidrogenoaren ekoizpena gas naturala (metanoa) erabiltzen duten prozesuen mende dago ( % 95), eta horrek esan nahi du 830 milioi tona karbono dioxido (CO2) isurtzen direla azpiproduktu gisa. Beraz, premiazkoa da hidrogenoaren ekoizpena deskarbonizatzeko moduak aurkitzea, CO2 isurien helburu globalak betetzeko.
Hidrogenoaren ekoizpena
Hidrogenoa unibertsoan ugaria den arren, hidrogeno askea ez dago erraz Lurrean. Hemen molekulei lotuta dago, ugarienak ura (H2O) eta hidrokarburoak dira, bereziki metanoa (CH4). Horrela, hidrogeno librea lortzeko, molekula horiek zatitu egin behar dira energia emanez, gero ura sortzeko oxigenoarekin birkonbinatuz berreskura daitekeena. Horregatik, hidrogenoa bektore energetiko gisa deskribatzen da, eta ez lehen mailako energia-iturri gisa.
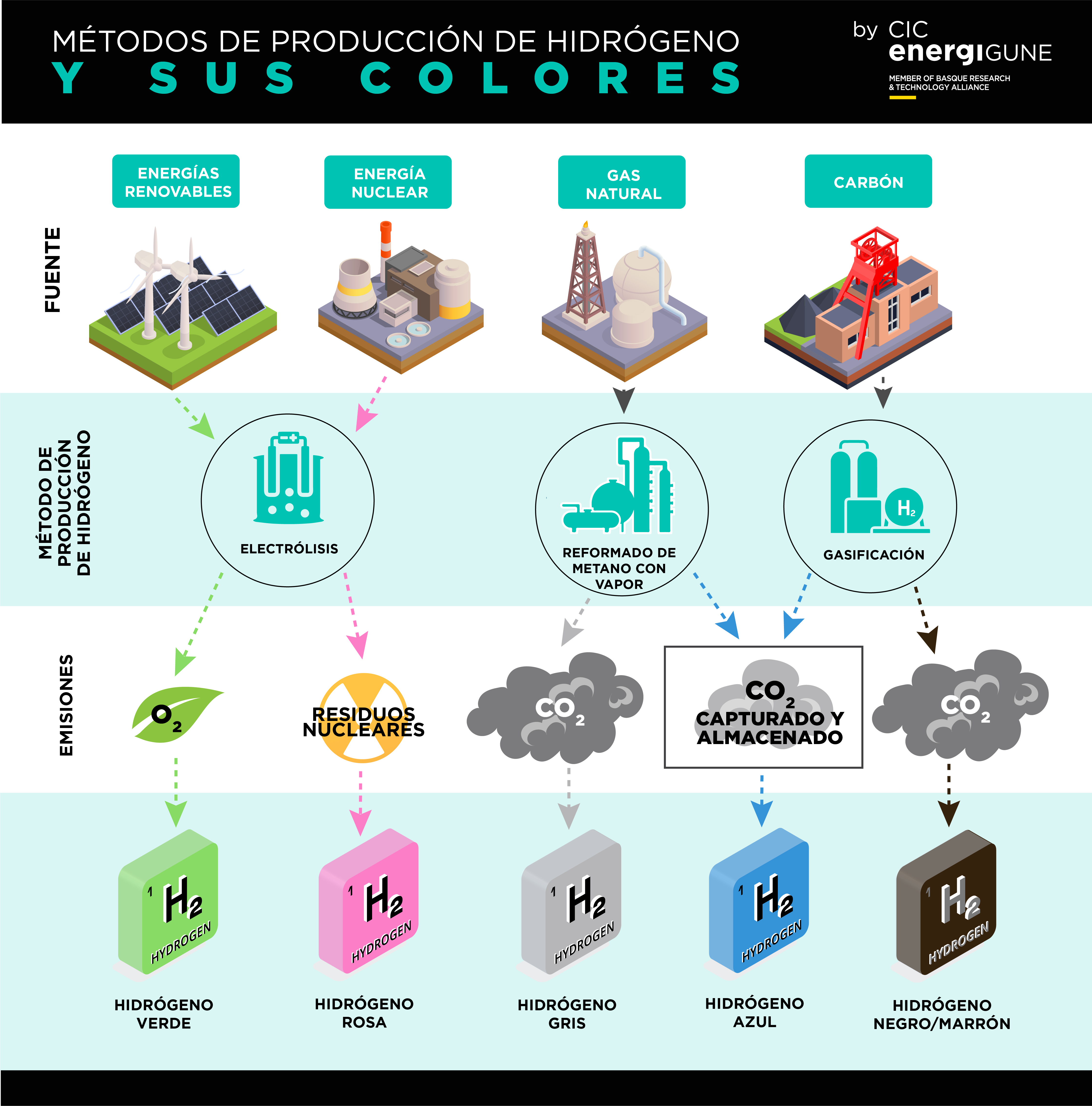
Nola sor daiteke hidrogenoa? Lehen mailako energia-iturri desberdinak dituzten ibilbide asko daude, argia, beroa, energia elektrikoa edo iturri horien konbinazioak izan daitezkeenak. Blogeko artikulu hau mugatuegia da hidrogenoa ekoizteko metodo guztiak barne hartzeko, bai erabiltzen ari direnak bai garatzen ari direnak, baina lehiakide nagusiak hartuko ditu barnean, eskala handian aplikatzeko.
Lehen metodoa, eta asko duena, unibertsalena da, gas naturalaren lurrunarekin eraberritua, askotan Metanozko Erreformatua Vapor bidez (SMR) bezala ezagutzen dena. Kasu honetan, lurruna eta gas naturala, kutsatzaileak ezabatzeko tratatuak, elkarrekin berotzen dira presio altuan ~ 900 ºC-tan nikelezko katalizatzaile baten gainean. Emaitza karbono monoxidoaren (CO) eta hidrogenoaren nahasketa bat da, syngas izenez ezagutzen dena. Syngasa, ondoren, gasa uretara aldatzeko erreakzio batean tratatzen da, hidrogeno eta karbono dioxido gehiago ekoizteko (ikus laukia xehetasun gehiagorako). Gaur egun, ekoitzitako CO2 atmosferara askatzen da, baina azpiproduktu gisa erabil daiteke, adibidez, elikagaiak prozesatu eta ontziratzean, non, berriz ere, atmosferara askatzen baita. Lurrun bidezko erreforma-prozesuak gas naturalaren errekuntzaren erreakzioa bultzatzeko behar den beroa lortzen du, CO2 gehiago sortuz.
|
Lurrun bidezko metanozko eraberritzea
Tenperatura eta presio altuetan, metanoak eta lurrunak hurrengo ekuazioan deskribatzen den bezala erreakzionatzen dute; CH4 + H2O -> CO + 3H2 Hidrogenoaren (H2) eta karbono monoxidoaren (CO) konposatuari syngas esaten zaio eta beste produktu batzuk sintetizatzeko erabil daiteke. Hidrogeno gehiago sor daiteke, syngasak gasetik uretara aldatzeko erreakzioa jasoz. Erreakzio hori jarraian agertzen da, tenperatura baxuagoetan. CO + H2O -> CO2 + H2 Orduan, prozesuaren erreakzio globala CH4 + 2H2O -> 2CO2 + 4H2 Metanoak eta urak 2 hidrogeno molekula ematen dituzte. - Hidrogenoa gas-nahasketa horretatik ateratzen da presio oszilazio bidezko adsortzio gisa ezagutzen den prozesu baten bidez, eta horrek beharrezko energia handitzen du (eta, beraz, CO2 isurketa). |
Lurrunarekin egindako erreforma-erreakzioari beroa emateko beste bide bat metanoaren oxidazio partziala da, erreakzioa gertatu ahala beroa sortzen duena. Oxidazio partzialeko erreakzioa lurrunarekin egindako erreforma-erreakzioari akoplatu ahal zaio, eraberritze autotermikoa (ATR) deritzona sortzeko (ikus laukia). Kanpoko berorik behar ez denez, eraberritze eraginkorragoa eta trinkoagoa da, eta horrek esan nahi du karbono gutxiago isurtzen dela (ikus, esate baterako, Johnson Mattheyren LCH).
Metanoan oinarritutako prozesu horiek deskarbonizatzeko, ekoiztutako CO2 biltegi geologiko batean harrapatu eta biltegiratu behar da. Karbonoa biltzeko, erabiltzeko eta biltegiratzeko proiektuek CO2 biltegi geologikoetan ponpatzea dakarte, hala nola petrolio- eta gas-hobi agortuetan. Adibide bat Erresuma Batuko ipar-mendebaldean dagoen HyNet hidrogeno sarearen garapena da.
|
Oxidazio partziala hidrogenoa sortzeko beste bide bat da. Metanoa oxigeno edo aire nahikoarekin nahasten da, syngasa sortzeko. Hori berriro prozesatu daiteke gasa uretara aldatzeko erreakzioaren ondorioz, hidrogeno gehiago sortzeko. 2CH4 + O2 -> 2CO + 4H2 Hidrogenoaren (H2) eta karbono monoxidoaren (CO) konposatuari syngas esaten zaio eta beste produktu batzuk sintetizatzeko erabil daiteke. Hidrogeno gehiago sor daiteke, syngasak gasetik uretara aldatzeko erreakzioa jasoz. Erreakzio hori jarraian agertzen da, tenperatura baxuagoetan. 3CH4 + O2 + H2O -> 3CO + 7H2 |
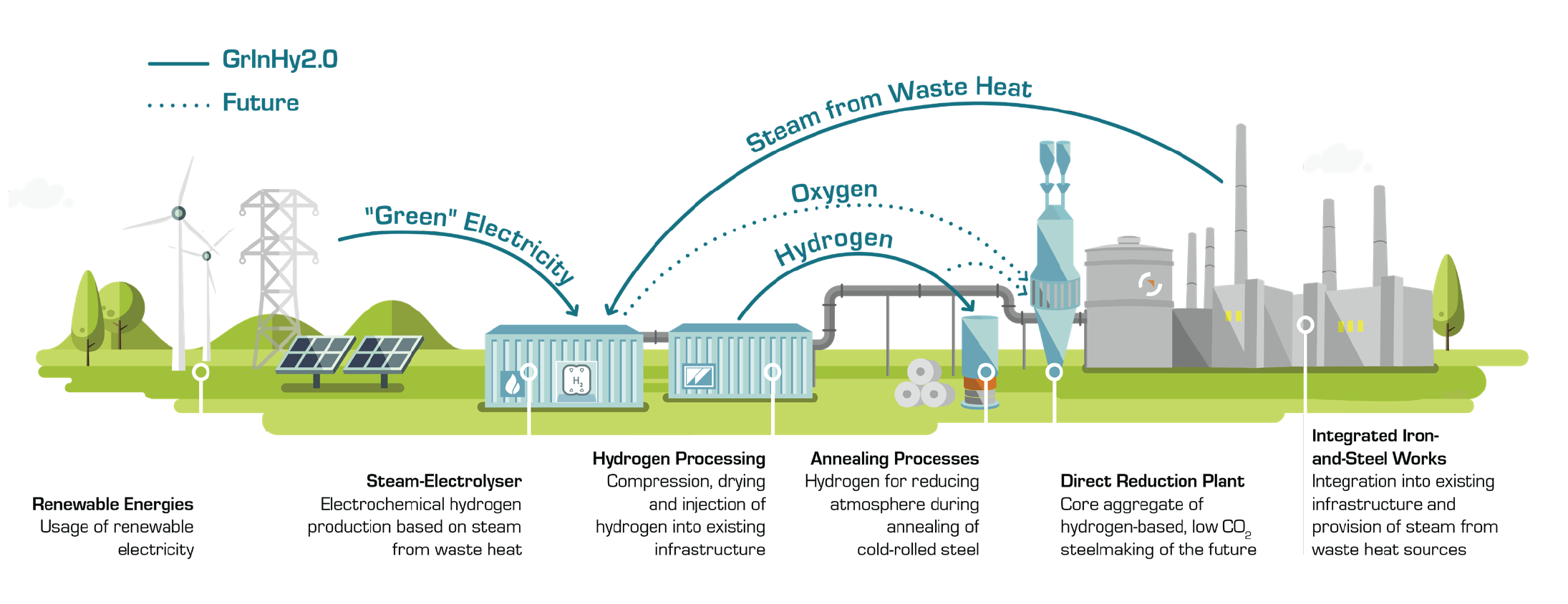
Indarrez sustatzen ari den bide alternatiboa uraren elektrolisiaren bidez hidrogenoa ekoiztea da, batez ere elektrizitate berriztagarria erabil badaiteke. Hau aurreko blog batean deskribatu zen hidrogeno berdearen ekoizpena bezala. GrInHy2.0 bezalako proiektuek hidrogeno berdea ekoiztea dute helburu, lehengai industrial gisa erabiltzeko.