Galdera hori ez da erraza erantzuten. Londresko Imperial Collegeko Tom Welton irakaslearen hitzetan,"...likido ioniko bat solido onik sortzen ez duen gatza da". Oro har, likido ionikoa, literalki, gatz likidoa, deskonposatu aurretik urtzen den (likido bihurtzen den) gatz gisa defini daiteke.
Likido ionikoak katioi eta anioi organiko eta ez-organikoz osatuta egon ohi dira. Material ioniko horiek bi taldetan sailkatzeari buruzko adostasun estentsibo baina eztabaidagarria dago: "giro-tenperaturan dauden likido ionikoak" deritzenak, 100ºC-tik beherako tenperaturan edo tenperatura berdinetan likido bihurtzen diren gatzak, eta askoz tenperatura altuagoetan urtzen diren "gatz urtuak" (adibidez, NaCl 803ºC-tan). Likido ionikoen sailkapen eztabaidagarri hori modu arbitrarioan oinarritzen da fusio-tenperaturetan, baina tipoen artean ere bereiz daiteke, bien aplikagarritasun praktikoan dauden desberdintasun nabarien arabera.
Artikulu honetan, "giro-tenperaturan dauden likido ionikoak", horien propietate bakarrak eta aplikazio-eremuak aztertuko ditugu.
Likido ionikotzat jotzen den lehen konposatuaren aurkikuntza Paul Waldeni egotzi dakioke, 1914an, bere taldeak lantzen zuen tenperaturan egoera likidoan ager zitezkeen gatz urtuak bilatzen ari zenean. Lehen likido ioniko hori etilamonio-nitratoa zen ([EtNH3] [NO3]), 12ºC-ko urtze-tenperaturarekin, eta literatura zientifikoan aipatu zen lehen likido ionikotzat jotzen zen.
Ondoren, likido ionikoen ikerketa eta potentzialaren aurrerapenak oharkabean igaro ziren denbora batez. Joan den mendeko 60ko hamarkadara arte ez zen sustatu likido ionikoen ikerketa, komandanteak (Dr.) zuzendutako AEBko Indar Armatuen Akademiaren hasierako ikerketa-proiektu bati esker: Lowell A. King. Orduan, helburu nagusia bateria termikoetan erabilitako LiCl/KCl-aren gatz urtuen elektrolitoen ordezko bat aurkitzea zen. Ordutik, Estatu Batuetako Indar Armatuen Akademiak etengabeko programa baten aldeko apustua egin zuen likido ioniko horiek ikertzeko. Programa horretan, hainbat likido ioniko garatu zituzten, ia lau hamarkadatan zehar katioi eta anioi desberdinak konbinatuz.
Taula honetan, 60 eta 90 urte bitarteko hamarkadetan aurkitutako likido ioniko garrantzitsuenetako batzuk ikus daitezke:
|
Likido ionikoa |
Urtea (ref.) |
|
|
[Et3NH][CuCl2] |
1963 (Inorg. Chem.,1963, 2, 1210) |
|
|
[N2222][GeCl3] and [N2222][SnCl2] |
1972 (J. Am. Chem. Soc., 1972, 94, 8716) |
|
|
[RPy][AlCl4] and [R2Im][AlCl4], R=alkyl] |
1982 (Inorg. Chem. 1982, 21, 1263) |
|
|
[R2Im][BF4] and [R2Im][PF6] |
1992 (Chem. Commun., 1992, 965) |
|
|
[R2Im][NTf2] |
1996 (Inorg. Chem. 1996,35,1168) |
|
|
Im = imidazolium, Py = pyridinium, NTF2 = bis(trifluoromethylsulfonyl)amide, N2222 = tetraethylammonium, EtPyBr = n-ethyl pyridinium bromide and Et3NH = triethyl ammonium. |
||
Geroago, XXI. mendearen hasieran, likido ionikoekiko eta haien aplikazio potentzialekiko interesak berpizkundea bizi izan zuen, eta komunitate zientifikoaren artean interesa bereganatzen hasi ziren. Interes hori argi eta garbi islatu zen argitalpen zientifikoen kopuruan, zeinetan likido ionikoa hitz gakoetako bat bezala agertzen baitzen. Hurrengo grafikoari begiratuz gero, batek ondoriozta dezake azken 10 urteetan (2012-2021) komunitate zientifikoak likido ionikoetan duen interesa (>54.000 argitalpen zientifiko) izugarri hazi zela, eta joera da datozen urteetan hazten jarraitzea (dagoeneko 3.000 argitalpen baino gehiago dira 2022an).
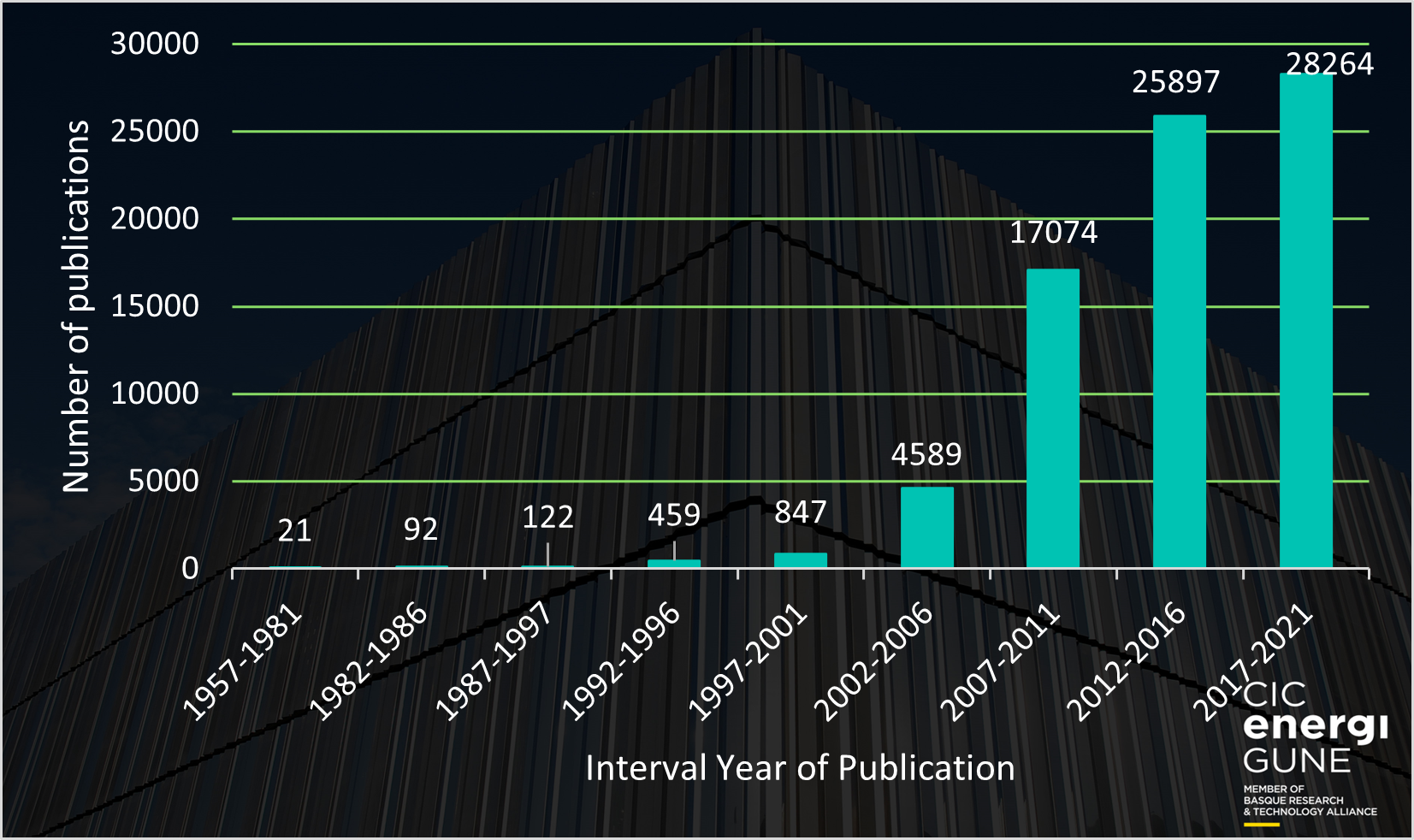
Likido ionikoek propietate bakarrak dituzte, aplikazio espezifikoetarako berezi egiten dituztenak. Izan ere, posible izango litzateke likido ionikoa ia edozein aplikaziotarako behar diren ezaugarriekin diseinatzea eta sintetizatzea, katioien eta anioien arteko konbinazio mugagabe posibleak direla eta.
Likido ioniko gehienek dituzten propietate bakarren artean, honako hauek azpimarra daitezke:
Oro har, likido ionikoek solido baten propietate tipikoak dituzte, nahiz eta likido egoeran egon. Ezaugarri horiez gain, likido ionikoak oso egokiak dira tresna sintetikoak erabiliz aldaketak egiteko; adibidez, kationean talde funtzionalizatuak sartuz edo aniona aldatuz, aplikazio berezi baterako nahi den ezaugarria hobetu edo sortzeko.
Berezko propietate horiek eta haien egokitzapen handiak hautagai bikain bihurtzen dituzte likido ionikoak, H2 sortzeko eremuan erabil daitezen erreakzionatzeko eta/edo ko-katalizatzaile gisa, eta energia termikoa biltegiratzeko fase-aldaketako material gisa.
Hurrengo irudiak likido ionikoen sintesian erabiltzen diren katioi eta anioi ohikoenetako batzuk erakusten ditu.
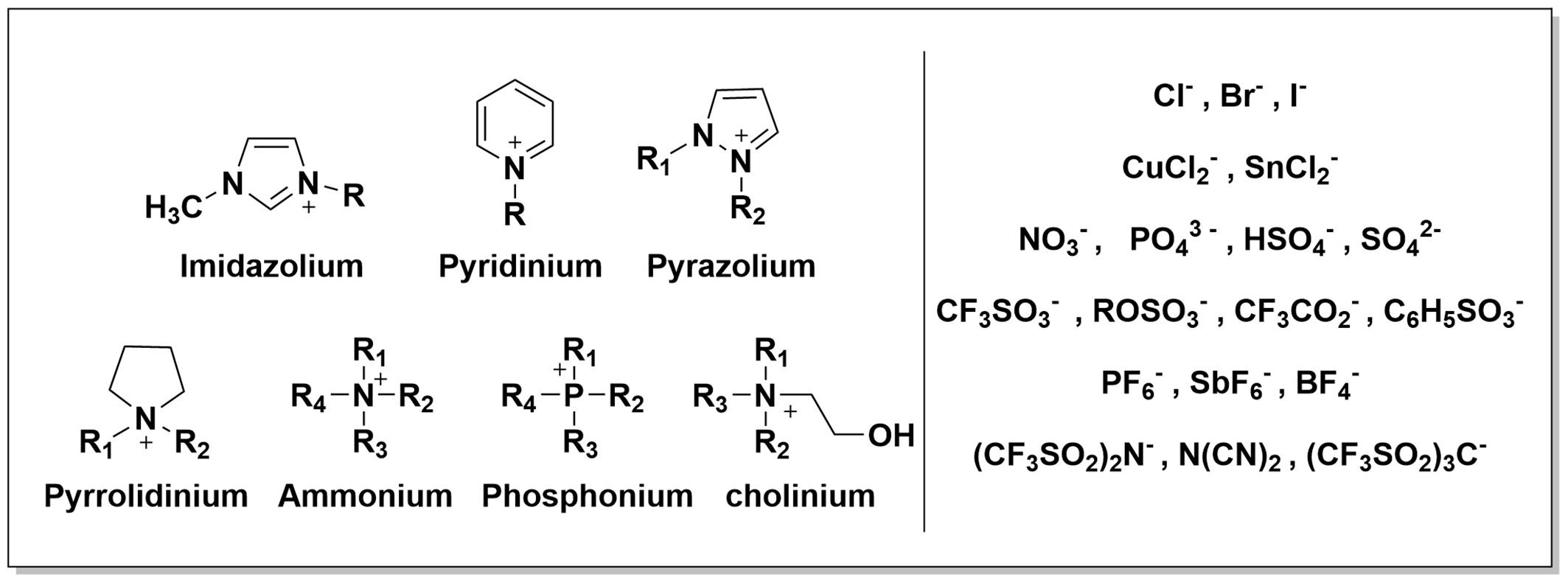
Likido ionikoak bi multzo handitan bana daitezke: likido ioniko aprotiko eta portikoa. Haren sintesia, katioi eta anioi hautatuetatik hasita, hainbat modutan gara daiteke:
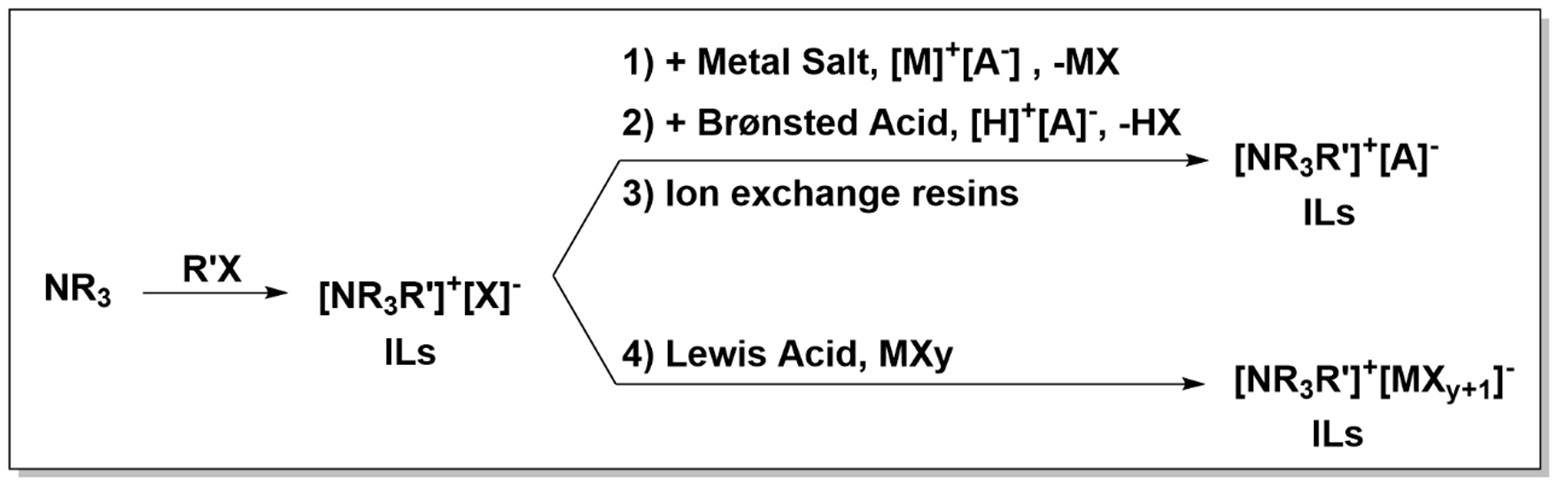
Oro har, likido ioniko aprotikoen sintesia aminak edo fosfinak (zati kationiko gisa) eta alkilo-haluroak (zati anioniko gisa) erabiliz hasten da, kuaternizazio-erreakzio baten bidez, eta ondoren, aukeran, truke anionikoko erreakzioak (adibidez, metatesi anionikoa).
Bestalde, likido ioniko protetikoen sintesia askoz errazagoa da, eta Brønsted azido baten eta Brønsted base baten arteko neutralizazio soilaren bidez lortzen dira. Katioia eta anioia hautatzea funtsezkoa da, eta likido ionikoen propietate termofisikoak eta, ondorioz, aplikazio-eremua zehaztuko ditu.
Gaur egun, IOLITEC (> 250 likido ioniko zorroan, g-tik kg-ra bitarteko eskala, > tona 1 2020an), PROIONIC (> tona 1), SCIONIX (kg eskala eta likido ioniko 1 > tona) eta SOLVIONIC (> 1,5 tona/hilabete 2021ean eta > 50 tona hilean) enpresek likido ioniko ugari fabrikatzen eta merkaturatzen dute. Azpimarratu behar da enpresa horiek guztiak oso aktiboak direla eta beren ikerketa eta garapenean inplikatuta daudela.
Likido ionikoek, beren propietate intrinseka bakarrak, kationaren eta anionaren arteko konbinazio ia mugagabeak eta horiek aldatzeko eta/edo funtzionalizatzeko erraztasun nahikoa dutenez, aplikazio posible ugari dituzte:

Ikus daitekeenez, likido ionikoen aplikazio-eremuek prozesuen teknologiatik hasi eta fluido funtzionaletaraino hartzen dituzte, elektrokimika, analitika, beroa garraiatzea eta bihurtzea, edo sintesia eta katalisia barne. Hala ere, likido ionikoak eratzeko aukeratutako katioi eta anioiak ia kalkulaezinak izan daitezkeenez, etorkizunean aplikazio potentzialak hazi egingo dira eta zientzialarien irudimenak soilik mugatuko ditu.
Pentsa daiteke, oker, likido ionikoen interes nagusia ikerketa-mailan dagoela. Baina material bakar horiek areagotu egin dute likido ionikoak beren prozesuetan sartu dituzten konpainia askoren interesa:
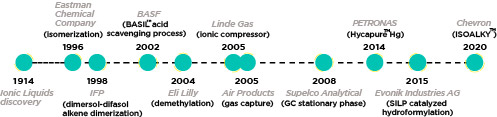
Oro har, adibide horiek erakusten dute likido ionikoetan oinarritutako teknologiak merkataritza- eta industria-mailan ezar daitezkeela, haien moldakortasunagatik eta aplikazio ugariengatik (ezagutzen direnak eta etortzeke daudenak). Hala ere, teknologia horien potentzial handiena iristeke dago oraindik, eta, merkataritzan dituzten propietate bakarrak ustiatzeko, funtsezko ikerketarekin industriek duten konpromisoak berebiziko garrantzia du.
CIC energiGUNEn, Energia Termikoko Soluzioen (TES) arloan, likido ionikoetan oinarritutako teknologia berriak diseinatu eta garatzen ditugu, hidrogenoaren ekoizpenean/biltegiratzean eta energia termikoaren biltegiratzean aplikatzekoak.
Likido ionikoetan oinarritutako sistema katalitiko disruptiboen diseinuari, garapenari eta karakterizazioari dagokienez, CIC energiGUNEn H2 purua eta karbono-material baliotsua lortu nahi izan genuen hondakin plastikoen dekonstrukzio katalitikotik abiatuta (HDPE, PP eta PS), ohikoak ez diren berotze-metodoen bidez.
Likido ionikoetan oinarritutako sistema katalitikoak funtsezkoak dira ikertutako prozesuan, eta honako hauek proposatzen dira: prozesu katalitikoaren errendimendua eta selektibitatea handitzea, egosketaren eta/edo sinterizazioaren zentro katalitiko aktiboak babestea, koproduzitutako karbono-material baliotsua berreskuratzea, zentro katalitiko aktiboak berreskuratzea eta berrerabiltzea, eta karbono-materiala eta H2 hutsa bereiztea erraztea.
H2 biltegiratzeko likido ioniko berrien diseinuari, garapenari, sintesiari eta karakterizazioari dagokienez, hidrogenazio/deshidrogenazio baldintzei aurre egiteko egonkortasun termikoa eta kimikoa duten likido ionikoetan zentratzen da ikerketa, hidrogeno likidoaren eramaile gisa erabiltzeko hidrogenoaren dentsitate grabimetriko nahikoarekin ( % 2-4).
"Kristal plastiko ioniko organikoen (OIPC)" (likido ionikoen azpimaila bat) diseinuari, garapenari, sintesiari eta karakterizazioari dagokienez, CIC energiGUNEn OIPCei buruzko ikerketa garatzen ari gara, energia handiko trantsizio solido eta solidoekin, tenperatura baxuko/ertaineko aplikazioetarako (etxeko eta industriako eremuak) bero sorra biltegiratzeko fase-aldaketako material gisa erabiltzeko. Halaber, ELKARTEK CICe21 proiektuaren eta abian den doktorego-tesi baten esparruan, gero eta ezagutza handiagoa lortzen ari gara OIPCen egitura kimikoaren eta fase-aldaketarako material gisa duten errendimenduaren arteko erlazioa ulertzean.
Zalantzarik gabe, likido ionikoak aparteko propietateak eta aplikazio potentzial mugagabeak dituzten materialak dira. Hala eta guztiz ere, oraindik ere erronka bat da aplikazio jakin baterako behar diren ezaugarriak bete ditzakeen katioia/anioia konbinazio egokia aurkitzea. Horregatik, CIC energiGUNEn, energia termikoa biltegiratzeko eta katalogatzeko aplikazio iraunkorragoetarako likido ionikoak ulertzeko eta garatzeko ikuspegi berriak lantzen ditugu, likido ionikoetan oinarritutako teknologia disruptiboetan aplikatzen direnak.

Egilea: Eduardo José García-Suarez, CIC energiGUNEren Biltegiratze Termikoaren arloko Fase Trantsizioak eta Portaera Kritikoak ikerketa-taldeko ikertzaile elkartua (Ikerbasque Research Fellow).




Energia biltegiratzeko azken joerak eta ikerkuntzako berrikuntzak ezagutu nahi badituzu, harpidetu zaitez.

Goi-mailako talde batean sartu nahi baduzu, hainbat diziplinatako espezialistekin elkarlanean aritu edo zure kezkak kontatu nahi badituzu, ez pentsatu bi aldiz...